Es un enlace químico que mantiene unidos los átomos (unión entre núcleos atómicos y los electrones de valencia, que se juntan alrededor de éstos como una nube) de los metales entre sí. Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas.
CARACTERISTICAS
Propiedades del enlace metálico
Las redes cristalinas
ENLACE METÁLICO
Se llama enlace metálico al tipo de unión que mantiene unidos los átomos de los metales entre sí. Estos átomos se agrupan de forma muy cercana unos a otros, lo que produce estructuras muy compactas. Se trata de redes tridimensionales que adquieren la estructura típica de empaquetamiento compacto de esferas. En este tipo de estructura cada átomo metálico está rodeado por otros doce átomos (seis en el mismo plano, tres por encima y tres por debajo).
Propiedades del enlace metálico:
Características de los metales:
1.- Suelen ser sólidos a temperatura ambiente, excepto el mercurio, y sus puntos de fusión y ebullición varían notablemente.
2.- Las conductividades térmicas y eléctricas son muy elevadas. (Esto se explica por la enorme movilidad de sus electrones de valencia)
3.- Presentan brillo metálico.
4.- Son dúctiles y maleables. (La enorme movilidad de los electrones de valencia hace que los cationes metálicos puedan moverse sin producir una situación distinta, es decir una rotura)
5.- Pueden emitir electrones cuando reciben energía en forma de calor.
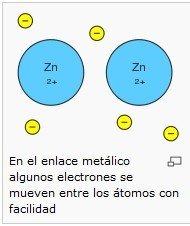
6.-Para explicar las propiedades características de los metales se ha elaborado un modelo de enlace metálico conocido como modelo de la nube o del mar de electrones:
7.- Los átomos de los metales tienen pocos electrones en su última capa, por lo general 1, 2 ó 3..
EJEMPLOS:
Los enlaces metálicos son a su vez enlaces covalentes por lo que es común que los átomos compartan algunos pares de electrones con los átomos a su alrededor, razón de la características arriba mencionadas. Cualquier cantidad de un elemento metálico en su forma pura es un ejemplo de enlace .iónico.
Ejemplos de enlaces metálicos:
Ejemplos de enlaces metálicos: mercurio.
Ejemplos de enlaces metálicos: Hierro.
Ejemplos de enlaces metálicos: Galio.
Ejemplos de enlaces metálicos: Cobre.
Ejemplos de enlaces metálicos: Aluminio.
Ejemplos de enlaces metálicos: Titanio.
Ejemplos de enlaces metálicos: Zinc.
Ejemplos de enlaces metálicos: Cadmio.
Ejemplos de enlaces metálicos: Oro.
Ejemplos de enlaces metálicos: Plata.
URL:
https://www.google.com.mx/webhp?sourceid=chrome-instant&ion=1&espv=2&ie=UTF-8#q=enlace+metalico+caracteristicas
http://html.rincondelvago.com/enlace-metalico.html
http://www.ejemplos.org/ejemplos-de-enlaces-metalicos.html
Autor: Omar Catzin.
mi conclusión de que en nuestra vida cotidiana, usamos muchas interacciones de moléculas o mejor conocidos como fuerzas intermoleculares sin que nosotros nos fijemos ya donde haya moléculas, hay interacciones intermoleculares.
ResponderBorrarPor ejemplo un vaso de agua, entre las moléculas de agua hay puentes de hidrogeno.
En los aceites hay fuerzas de London solamente por que son compuestos no polares, en las bebidas alcoholicas, hat interacciones dipolo-hipolo, y puente de hidrogeno entre el agua y el etanol, o ion-dipolo entre agua y sal.
Usamos muchas cosas con fuerzas intermoleculares, sin que nos demos cuenta, casi todo lo que no rodea tiene esa interaccion de molecula con molecula para formar algún compuesto que nosotros utilizamos.
Sim embargo nosotros no sabemos cual es cual, de las fuerzas intermoleculares como las del puente de hidrogeno, puente de London entre otros.
Pero nosotros los utilizamos sin un conocimiento adecuado y solo en cosas comunes de nuestra vida cotidiana.
Mi conclusión es que esto me ayuda a mi asco de tarea asi que Grafiaz
ResponderBorrarGeniÑ
ResponderBorrarl
ResponderBorrarGRACIAS POR LOS DATOS Y RESUMEN........ ME AYUDARÁ MUCHO
ResponderBorrarMe ayudó bastante con mi tarea....busaue en libros y me confundía...pero ahora veo que redactaste muy buen la información.
ResponderBorrar